

 字體:小 中 大
字體:小 中 大 |
|
|
|
| 2021/07/21 11:22:54瀏覽829|回應0|推薦4 | |
| 資料來源與版權所有:肝病防治學術基金會 B肝疫苗問世40年—台灣率全球之先注射疫苗 走出B肝帶原宿命 撰稿╱楊培銘(肝病防治學術基金會總執行長、臺大醫學院名譽教授) 1981年B型肝炎疫苗問世,台灣率先實施新生兒B肝疫苗注射,將台灣人感染B肝病毒之宿命根除,更證實透過B肝疫苗注射能有效預防肝細胞癌之發生,這個劃時代的成果,讓國際驚艷並群起效法,世界衛生組織(WHO)更參考台灣的成功經驗,訂定全球嬰幼兒全面施打B肝疫苗政策。值此B肝疫苗上市40年之際,撫今追昔,特為文紀念諸多高瞻遠矚深具遠見的前輩,克服種種困難,使消滅B肝得以在台灣實現。  肝炎可分傳染性和非傳染性,其中傳染性肝炎主要是由肝炎病毒所導致。 肝炎病毒主要有五種,稱為A、B、C、D、E型肝炎,其中A、E型肝炎是經口傳染,B、C、D型肝炎則是由體液傳染(血液和生殖液)傳染。 早年每5人有1人是B肝帶原者 肝病是台灣的國病,主因是B型肝炎病毒導致的慢性肝炎,在新生兒B肝疫苗注射實施前,台灣的成年人有15~20%為B型肝炎病毒帶原者,在全世界數一數二,其中約一半是由帶原的媽媽於生產過程中傳染給新生兒,過去稱為垂直傳染、周產期或母嬰傳染。另外一半則主要是在學齡前(小於6歲)經由打針得到感染。 針對傳染途徑已被明確瞭解的疾病,最佳之道乃是預防,若能研發出疫苗,則疫苗注射應為最佳的預防方式。 B型肝炎病毒是一種DNA病毒,它的病毒顆粒包覆在外套之內,這個外套上面佈滿所謂表面抗原的蛋白質,很幸運的是,B肝病毒表面抗原很少發生突變,且在各種血清型或基因型的B肝病毒間皆無明顯差異,因而在B肝病毒結構被完全瞭解後,順利研發出來的疫苗才能具有很高的效益,不必辛苦地一再研發新的疫苗。相反的,RNA病毒則會迅速地一直突變,若不是需要一再研發新的疫苗(如:流感病毒),就是不容易研發出疫苗(如:C型肝炎病毒)。 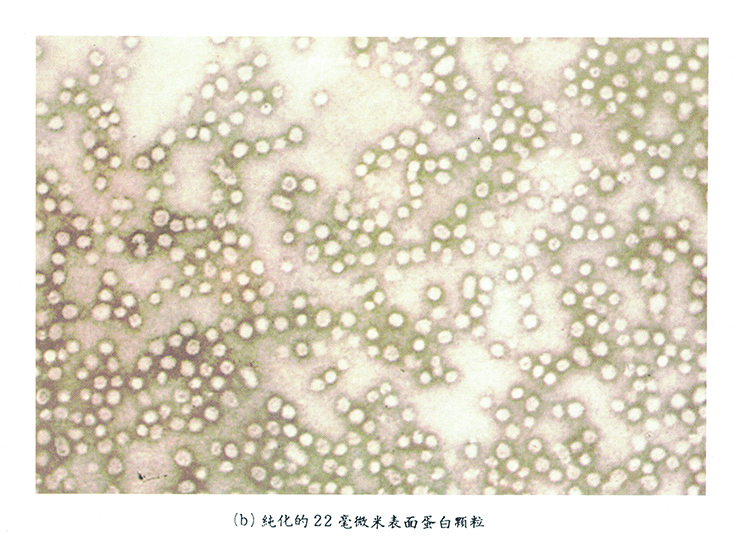 【圖說:將B肝帶原血漿經過一系列處理後,得到純化的22毫微米表面抗原蛋白顆粒。】 1981年B肝疫苗上市 新生兒注射臨床試驗一波三折 在分子生物學技術建立及普及之前,B型肝炎疫苗只有血漿疫苗,那是將B肝帶原者之血漿加以嚴謹的處理,務必消除血中可能存在的各種傳染及有害物質,而後純化出B肝病毒的表面抗原。將表面抗原打入黑猩猩體內會誘發其體內產生表面抗體,這種抗體可以將侵入體內的B肝病毒中和消滅且能避免B肝病毒感染肝細胞;在動物實驗確認其效能及安全性後,才能進入人體試驗,經過層層關卡驗證此等疫苗在人體注射之效能及安全性,才能在相關主管機關之認證下准予上市。 1981年間,美國默克及法國巴斯德兩家藥廠的B型肝炎疫苗陸續獲准上市,因而台北榮民總醫院羅光瑞教授與法國巴斯德藥廠於當年10月簽約進行新生兒臨床試驗,畢斯理教授和臺大醫院李慶雲教授則於11月與美國默克藥廠簽約進行新生兒臨床試驗。在此之前,血漿B型肝炎疫苗之新生兒臨床試驗其實是歷經一番波折才獲准通過的。 事實上,1981年2月衛生署本已核准默克藥廠的B型肝炎疫苗在台灣進行兒童臨床試驗,計畫主持人是曾任美國海軍第二醫學研究所專門研究B型肝炎傳染途徑的畢斯理教授,不料卻引起民眾和醫界之質疑,且在媒體上大肆撻伐,認為把台灣孩童當白老鼠,更擔心血漿疫苗的安全性,尤其當時才被發現的愛滋病毒是否會潛藏其中,因為血漿來源可能取自愛滋病患。當時監察院覺得事態嚴重,由尤清和王爵榮兩位委員負責調查,他們在臺大醫院檢驗大樓7樓的會議室中,對陳定信教授質詢了4小時,態度才由剛開始的咄咄逼人轉為支持,其後在調查報告中指出問題核心:衛生署應該儘速建立台灣的臨床試驗規範,且應於國外藥廠在該國通過B肝疫苗上市,取得銷售執照後,才能進口台灣做臨床試驗,且試驗對象應該是新生兒,而非4~6歲的兒童。幸而默克藥廠及巴斯德藥廠之B肝疫苗在不久之後陸續順利在美國和法國上市。 B肝疫苗決策背後英雄 1984年7月,台灣領先全世界對B肝帶原孕婦的新生兒實施B肝疫苗注射,更於1986年7月擴大至所有新生兒;由於其後所觀察到的成效卓著,世界各國陸續仿效實施。這個決策的關鍵人物是時任行政院政務委員暨科技顧問組召集人的李國鼎先生,他認為國家不應只注重經濟發展,更應注重國民健康,而B型肝炎是國病,影響國人生命甚鉅,因此B型肝炎防治正是國民健康大業,必須致力推動。時任行政院長的孫運璿先生也支持李國鼎先生的看法,將之列為國家重要政策。當時說服他們做成此等影響台灣新生代健康甚大的決策者,乃是宋瑞樓教授和陳定信教授,而其背後支撐則為台灣肝病醫學界和全球肝病權威。宋、陳兩位教授當時是如此說動李國鼎先生的:「疫苗政策每拖一年,就會增加約3萬名新生兒帶原者」。 即使如此,其後續發展並非一帆風順,雖然1981年10月及11月兩個B型肝炎疫苗的新生兒臨床試驗已獲准進行,反對B肝疫苗注射的聲浪仍波濤洶湧,蠢蠢欲動。為了化解國內紛歧,李國鼎先生率領行政院科技顧問組站上第一線,於1981年11月10~11日主辦一場空前的「病毒性肝炎研討會」,主持人是科技顧問美國紐約大學校長Bennett教授,邀集世界知名肝炎權威及台灣肝炎專家齊聚一堂,終於弭平歧見。  臨床試驗證實疫苗效果顯著 新生兒臨床試驗證實B肝疫苗注射能有效阻斷母嬰傳染。畢斯理教授自1972年來台之後,即致力於B型肝炎傳染途徑之研究,發現台灣B肝盛行之主因為母嬰傳染,尤其是血中B肝病毒e抗原陽性的帶原孕婦,其所生嬰兒高達90%會變成B肝帶原者。這些新生兒於出生後24小時內接受B型肝炎免疫球蛋白(乃高單位B肝病毒表面抗體輸液),再於產後一週至6個月之間接受3劑(默克疫苗)或4劑(巴斯德疫苗)B肝疫苗注射,可將這些高危險群之新生兒帶原率降至6%,此等預防效果令人驚艷。 臨床試驗成果如此優異,且安全性極高,大家當然希望趕快制訂政策全面開打,但問題是經費!當時B肝疫苗剛問世,因此非常昂貴,每劑價錢高達20~40美元,為了減少財務衝擊,衛生署負責本案的許須美科長(陳定信教授夫人)銜命與藥廠殺價,最後降價為每劑4美元,預估每年要花3億元新台幣才能免費為所有新生兒注射B肝疫苗。經過這些努力之後,「B型肝炎預防注射實施計畫」草案終於在1983年11月10日經許子秋署長簽署通過後出爐,再經俞國華行政院長核准,裁定於1984年7月1日起免費給B肝帶原孕婦之新生兒注射B肝疫苗,試辦兩年後,於1986年7月1日起推廣至所有新生兒。 實施初期,陳定信教授和許須美科長到處奔波宣導,大力推展,加上全國上下醫療人員之努力,於18個月內新生兒接受注射比率已達95%,其後更慢慢上升至99%。  【圖說:現行B肝疫苗為基因工程技術製成。】 1990年基因重組 B肝疫苗問世 1980年代後半段,分子生物學技術漸趨成熟,因而開始出現基因重組疫苗,以基因工程技術在培養皿中利用酵母菌大量製造B肝病毒表面抗原,再予以純化,成為基因重組疫苗,接受B肝疫苗注射可能衍生的感染風險從此煙消霧散。1990年2月底,衛生署首度核准比利時史克公司生產的基因重組B肝疫苗在台上市,取代血漿疫苗,後者正式走入歷史。 35歲以下台灣新生代 B肝帶原降至1%以下 40年之後,臺大醫院張美惠教授持續追蹤的研究,顯示台灣的B肝帶原率已由原先之15~20% 降至1% 以下,以台北市城中區(現在改制為中正區)觀之,5歲以下孩童之B肝帶原率於1989年時已由1984年之9.3% 降至2%,2009年時更降至0.9%。特別令人高興的是,兒童肝細胞癌(100% 與B肝病毒相關)之發生率早已由1984年之每十萬人有0.54個病人,大幅降至1994年之每十萬人僅有0.20個病人(風險比降低至0.36)。這些傲人的成果不僅印證了於新生兒至6個月大期間之B肝疫苗接種,可有效阻斷B肝病毒之傳染,更證實了透過B肝疫苗注射可以有效預防肝細胞癌之發生。B肝防治計畫的成功,是台灣公衛史上的一大成就,也是全球B肝防治的典範。  【圖說:新生兒接種B肝疫苗是台灣公衛史上一大成就。】 接種B肝疫苗 約10%無法產生B肝抗體 不過,接受完整的B肝疫苗接種後,約有10% 的人無法產生B肝表面抗體,故過去二、三十年研究人員持續在研發新的B肝疫苗,包含DNA疫苗、mRNA疫苗、腺病毒載體疫苗等,但至今尚未能有所突破,更不用說能研發出只要打一劑的B肝疫苗。至於疫苗接種失敗且不幸仍成為B肝帶原之孩童,研究發現大多數是因其母親於生產前血中病毒量仍甚多(>106 IU/mL),因此現在健保針對懷孕達28週之B肝帶原孕婦,若其血中B肝病毒量>106 IU/mL,有給付抗病毒藥物惠立妥直到產後28天,過去的研究已證實,如此可將B肝疫苗無效不幸變成帶原者之機率減至極低,當然也會將肝細胞癌之發生率降得更低。 B肝疫苗為台灣疫苗工業奠下基礎 值得一提的是,在新冠肺炎病毒肆虐之際,台灣也有能力製造對抗新冠病毒的疫苗,乃是拜B肝疫苗之賜。因為B肝疫苗非常昂貴,長遠來看,台灣應該自己生產B肝疫苗才合理,因此在1984年行政院科技顧問組和國科會於經濟部下成立財團法人生物科技開發中心,且於同年在新竹科學園區成立保生公司,設立疫苗製造工廠,接受巴斯德藥廠血漿B肝疫苗製造之技術轉移。雖然後來因基因重組疫苗之興起而於1992年停工,但台灣的疫苗工業根基已在當時建立了,讓台灣在這個疫苗掛帥的年代不會缺席,前人的先知灼見,令人佩服。 |
|
| ( 知識學習|健康 ) |









