字體:小 中 大
字體:小 中 大 |
|
|
|
| 2021/06/04 07:38:37瀏覽9363|回應14|推薦31 | |
Pfizer/BioNTech seek full FDA approval for their Covid-19 vaccine 莫德納六月二日向美國食品暨藥物管理局申請全面批准其研發的COVID-19疫苗,成為第2家尋求監管機關核准並廣泛使用的藥廠。目前莫德納在美國只取得緊急使用授權。 莫德納(Moderna Inc)的競爭對手美國藥廠輝瑞(Pfizer Inc)和其合作夥伴德國生技公司BioNTech,已於數週前向美國食品暨藥物管理局(FDA)申請全面批准使用它們研發的2019冠狀病毒疾病(COVID-19)疫苗。 新聞引用至此~
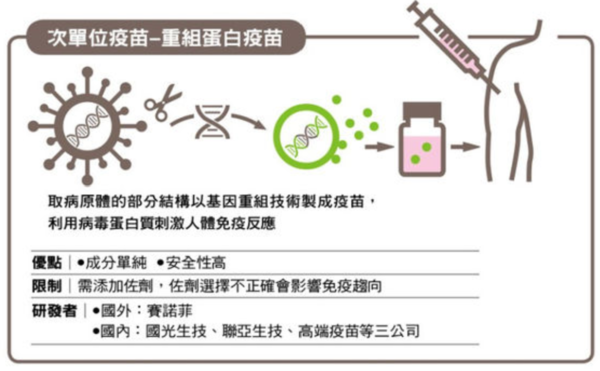
圖片來源:康健雜誌 根據CNN五月七日的新聞,輝瑞藥廠已經正式向美國食物及藥品管理局(FDA﹚提出新冠疫苗的藥證申請,也就是Full Approval。莫德納也隨後在六月二日向美國FDA提出藥證審查申請。輝瑞跟莫德納正式申請藥證,到底代表什麼意義呢? 首先,能申請藥證,代表這兩家疫苗都已經做完三期(有可能部分針對不同年齡疾病跟人種的三期還在進行,但完成的三期數量已經符合美國FDA規範,也提出足夠的數據證明疫苗有效性,才有可能讓美國FDA開始審查)。 第二,因為全球疫苗需求而實施的緊急使用授權(EUA),將會在第一家廠商拿到藥證之後功成身退,也就是說,只要有一個拿到藥證,根據緊急授權的精神,就不會再核准任何尚未拿到EUA的疫苗。 所以不管是台灣的高端聯亞國光,或是各國現在正在開發的數百家疫苗廠商,以後幾乎不可能再拿到美國FDA、歐盟EMA或是WHO的緊急授權,只能正式申請藥證,審查標準會嚴格很多! 高端聯亞就算拿到台灣食藥署的EUA,到時還是只能向美國及歐盟申請藥證,而已經有藥證的廠商必然全力阻撓,如果沒有辦法證明自己的疫苗比已經上市的疫苗更好更有效副作用更低,拿到藥證會是漫長的奮鬥! 高端聯亞,來得及嗎?誇口今年底一家要生產一億支,沒有藥證要賣給誰呢? |
|
| ( 時事評論|政治 ) |