字體:小 中 大
字體:小 中 大 |
|
|
|
| 2021/05/27 06:29:53瀏覽8748|回應11|推薦33 | |
蔡英文視察高端疫苗~中國時報攝
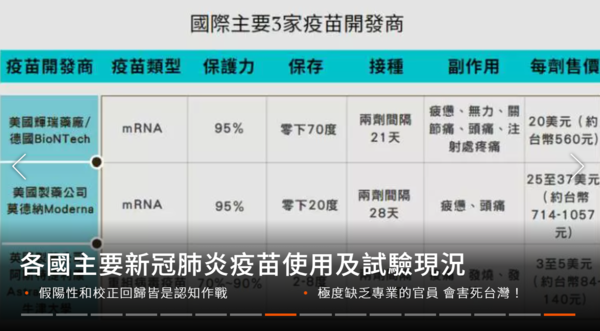
版主之所以找這些資料,是因為民進黨跟1450最近大規模發動針對台灣自己民眾的「認知作戰」,還有很多綠營人士發表關於新冠疫苗的假消息,所以版主今天為大家整理一下現在市面上主要使用及通過WHO認證的新冠疫苗,讓大家有清楚的比較,不要再被綠營騙了! 輝瑞﹨BNT﹨復必泰疫苗 輝瑞製藥與BioNTech於2020年11月18日公布疫苗在第三期臨床測試的有效率達到95%,隨後於11月20日向美國食品藥物管理局(FDA)申請緊急授權使用許可,美國食品藥物管理局於12月11日宣布批准緊急使用BNT162b2疫苗,並於2020年12月31日成為世界衛生組織首款核准使用的預防嚴重特殊傳染性肺炎疫苗。輝瑞與BioNTech在2021年4月1日發表跟進接種者6個月的研究報告,在收集12,000名完成兩劑疫苗注射並超過6個月的人士的數據進行分析後,顯示疫苗在現實世界的有效率為91.3%,並且沒有出現嚴重副作用,而有效率在所有年齡、性別及種族都大致相同。 目前綠營在網路上的認知作戰是,告訴台灣民眾上海復星賣的BNT疫苗, 中文名稱復必泰是在中國生產,且是BNT停止開發的BNT162b1候選疫苗,但事實上海復星代理的疫苗是BNT162b2,而且是在德國生產。最近南投縣長想買上海復星代理的BNT疫苗,結果行政院中部聯合服務中心執行長蔡培慧說,輝瑞送到中國的是疫苗原液,所以要分裝,就像手機組裝一樣要代工,還說這種代工疫苗才叫做復必泰?實在讓人覺得此人水準低,連常識也缺乏!其實一查就知道,上海復星只有代理BNT疫苗,目前也都在德國生產,銷給上海復星的BNT中文包裝名稱就叫復必泰,就像Panadol在台灣賣包裝就叫普拿疼一樣!另外,BNT疫苗在出貨玻璃瓶中就是濃縮原液,只有在施打時必須稀釋,出貨並不需要分裝,蔡培慧能夠找到沒人證實的資料,就請她公布一下證據吧! 莫德納嚴重特殊傳染性肺炎疫苗(代號:mRNA-1273,商品名:Moderna COVID‑19 Vaccine,簡稱:莫德納疫苗﹚ 美國國家過敏和傳染病研究所、生物醫學高級研究與開發管理局和莫德納合作開發的嚴重特殊傳染性肺炎疫苗,為一種信使核糖核酸(mRNA)疫苗,在2020年12月發表的第三期臨床試驗報告顯示該疫苗的有效率達94%。該疫苗需要以肌肉注射方式接種兩次,每次的劑量為0.5毫升,兩次之間相隔4週。2020年12月18日,mRNA-1273獲得美國食品藥品管理局核發緊急使用授權,其後在2020年12月23日在加拿大、2021年1月6日在歐盟、2021年1月8日在英國,獲發出緊急使用授權。世衛組織於2021年4月30日將該疫苗列入緊急使用清單。莫德納在2021年4月13日表示,追蹤超過3萬名已經接種兩劑疫苗的第三期臨床試驗參與者6個月後,至4月9日有900宗確診個案,顯示疫苗在6個月後的整體有效率仍達到90%,而預防重症的效力則為95%。 牛津-阿斯利康嚴重特殊傳染性肺炎疫苗(商品名:Vaxzevria、Covishield,簡稱阿斯利康疫苗、牛津疫苗、AZ疫苗,代號AZD1222) 英國牛津大學與阿斯利康製藥合作研發,以非複製型病毒載體為技術基礎,是一款針對嚴重特殊傳染性肺炎的預防疫苗,英國藥品及保健品管理局於2020年12月30日批准該款疫苗的緊急授權使用許可,歐洲藥品管理局亦於2021年1月30日批准該款疫苗在歐盟使用,該款疫苗於2021年2月15日獲世界衛生組織列入緊急使用清單,並成為世衛組織全球疫苗分配計劃(COVAX)首種發放的疫苗。這種疫苗的生產地在全球分布廣泛,包括英國、比利時、荷蘭、義大利、印度、韓國、日本、澳洲等國家。阿斯利康疫苗在涵蓋2.4萬人的第三期臨床測試中,有效率平均達到70.4%,最高可達90%。 嬌生嚴重特殊傳染性肺炎疫苗(英語:Johnson & Johnson COVID-19 vaccine) 由位於荷蘭萊頓的楊森疫苗及其比利時母公司同時也是美國嬌生公司的子公司楊森製藥研發的嚴重特殊傳染性肺炎疫苗。 它是一種基於人類腺病毒的病毒載體疫苗,人類腺病毒經過改造後會含有能產生嚴重急性呼吸道症候群冠狀病毒2型病毒尖峰蛋白的基因。人體的免疫系統會對這種尖峰蛋白產生反應並產生抗體。人類只需注射一劑該疫苗,且該疫苗無需冷凍保存。 該疫苗的臨床試驗於2020年6月開始,三期試驗涉及約4.3萬人。2021年1月29日,楊森公司宣布,在疫苗接種28天後,該疫苗預防嚴重特殊傳染性肺炎的有效率為66%,預防重症嚴重特殊傳染性肺炎的有效率為85%,預防嚴重特殊傳染性肺炎引起的住院或死亡的有效率為100%。 該疫苗於2021年2月27日獲得美國食品藥品監督管理局的緊急使用授權,2021年3月11日獲得歐洲藥品管理局的有條件上市授權。 看完歐美疫苗,我們來看看大陸經過WHO認證的疫苗 國衛疫苗﹨眾愛可維(代號:BBIBP-CorV ) 中國醫藥集團北京生物製品研究所(BBPI)研發的一款2019冠狀病毒病疫苗,該疫苗採用滅活SARS-CoV-2病毒(Vero細胞)技術,獲得有世界衛生組織緊急使用認證 2020年7月16日,國藥集團開始在阿拉伯聯合大公國對31000名志願者進行三期疫苗試驗。2020年12月9日,阿聯衛生部表示三期臨床試驗數據的中期分析顯示該疫苗有效率達到86%,中和抗體陽轉率99%,預防中度和重度病例有效性為100%,並宣布阿聯正式批准註冊該疫苗。2020年9月,巴林參與了該疫苗的三期臨床試驗,巴林王儲以志願者身份帶頭接種,約7700餘名志願者參與此次疫苗臨床試驗。除阿聯、巴林外,該疫苗還在埃及和約旦進行了三期臨床試驗。 以上就是通過WHO認證的新冠疫苗,這些疫苗通通都做過三期試驗且結果合乎WHO的標準。那麼台灣的疫苗呢? 台灣目前有聽說的兩支疫苗分別是高端及聯亞,至2021年5月為止,這兩支疫苗都只完成第二期人體試驗約4000~5000人的注射,且結果尚未公布。但是蔡英文卻已經告訴國人七月要開打了?這兩支連三期都沒做的疫苗,如果台灣批准緊急使用,其實也就是拿台灣人來做三期試驗,版主相信會有人願意當白老鼠,但版主是絕對不會嘗試的! PS;WHO認證疫苗的標準很簡單,第一就是疫苗效力須達50%以上,第二就是生產過程必須符合一定標準。聽起來簡單但目前也只有上述幾個疫苗達標!台灣的疫苗想跳過三期獲得認證的可能性幾乎是零! |
|
| ( 時事評論|政治 ) |