資料來源與版權所有:肝病防治學術基金會 翻轉晚期肝癌! 第一線治療藥物「免疫加標靶」 健保給付了!
諮詢╱許駿(臺大醫院癌醫中心分院教學研究部主任、臺大醫學院腫瘤醫學研究所特聘教授) 撰稿╱黃靜宜 免疫加標靶藥物組合是晚期肝細胞癌(以下簡稱肝癌)
的第一線療法,也是目前最強效的藥物,有5%的人肝腫瘤有機會
消失。
健保自2023年8月起納入給付,病人將可省下數十萬至數百萬元的藥費!哪些人可以使用?與其他治療方式如何搭配?

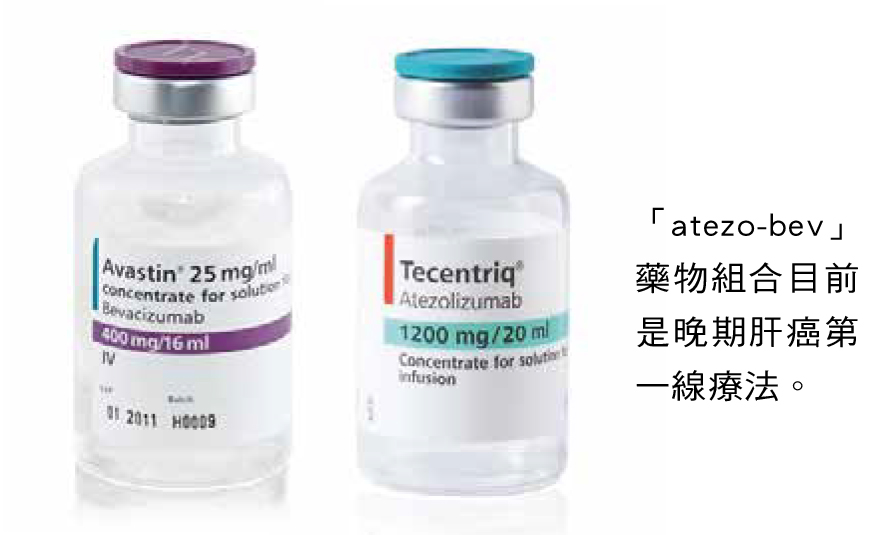
衛福部於2020年8月核准免疫加一種特定的抗血管新生標靶藥物,即atezolizumab+bevacizumab這款藥物組合可作為晚期肝癌的第一線療法,當時俗稱為A+B或double A,但高昂的藥費阻卻了不少病人接受最新標準治療的機會。在病人殷殷期盼下,終於在2023年8月納入健保。健保署發布新聞稿指出,預估約有2072位病人受惠,每位病人每年約可省下300萬元之藥費。
此款藥物組合中,免疫藥物的學名為atezolizumab、商品名Tecentriq(癌自禦);標靶藥的學名為bevacizumab,目前除原開發藥廠的Avastin(癌思停)外,另有Zirabev(力癌停)、Alymsys(艾麥斯)、Onbevzi(安備咨)這幾款生物相似性藥品(bio-similar)經衛福部核准上市。根據衛福部食藥署說明,所謂生物相似性藥品乃是與我國核准之原開發廠商之生物藥品(或參考藥品)高度相似之生物製劑,在品質、安全、療效上,與參考藥品無臨床上有意義的差異(no clinically meaningful differences)。
免疫加標靶 三成病人腫瘤縮小
目前晚期肝癌第一線藥物療法,經由隨機分配臨床試驗證實療效,得到美國FDA核准上市,並且列入國際肝細胞癌臨床診療指引的處方,共有蕾莎瓦(sorafenib)、樂衛瑪(lenvatinib)、A+B,以及雙免疫療法組合durvalumab + tremelimumab 四種。前三種台灣已上市且都有健保給付,但健保規定這三種只能擇一使用,且不得互換(指在健保體制下,自費不限)。
病人該如何選擇?根據臨床試驗的結果,接受A+B組合治療的326位受試者,反應率(objective response rate,簡稱ORR,也就是腫瘤會顯著縮小的比率)為27.6%,其中5.5% 為完全緩解。病人整體存活(overall survival, OS)期間中位數可延長至19.2個月(對照組以蕾莎瓦治療的整體存活時間中位數為13.4個月)。所以,當與病患及家屬討論藥物治療選擇時,如果病人符合健保給付條件,通常會優先選擇A+B。
用過健保給付之蕾莎瓦、樂衛瑪
不能再申請健保給付A+B 根據現行條文,A+B
的健保給付條件為:適用於治療轉移性或無法手術切除且不適合局部治療或局部治療失敗之晚期肝癌患者,肝硬化分級為Child-Pugh A級 ,且未曾接受全身性療法者(也就是過去沒有用過蕾莎瓦或樂瑪衛)。
患者還必須符合以下條件其中之一:
1.有肝外轉移(遠端轉移或肝外淋巴結侵犯)。
2.大血管侵犯(腫瘤侵犯門靜脈主幹或侵犯左/右門靜脈第一或第二分支)。
3.經導管動脈化學藥物栓塞(TACE)治療失敗者,需提供患者於12個月內大於等於3次局部治療的紀錄。
另外,需排除以下任一情形者:
1.曾接受器官移植。
2.正在接受免疫抑制藥物治療。
3.有上消化道出血之疑慮且未接受完全治療(需有半年內之內視鏡評估報告)。
另需注意以下事項:
1.與蕾莎瓦、樂衛瑪僅得擇一使用,不得互換。
2.atezolizumab+bevacizumab治療失敗後,不得申請使用regorafenib(癌瑞格)或ramucirumab(欣銳擇)。
需排除部分病人的原因
之所以規定必須附上病人近期的內視鏡報告,是因為bevacizumab這個藥物有引發出血的風險,且當初A+B的臨床試驗就有要求受試者需先做胃鏡,排除具有出血風險者。
接受過器官移植者,不建議使用免疫加標靶,主要是擔心會增加發生器官排斥的機會。此外,因為罹患自體免疫疾病使用免疫抑制劑治療的病患,沒有機會納入過去肝細胞癌的免疫治療臨床試驗。因此,這個病患族群使用A+B治療或其他免疫藥物治療,還沒有很完整的療效與安全性資訊可供參考。
如果病人不符上述健保給付條件,還是想用免疫加標靶,就只能自費;要不要花這筆錢,需和家人、醫師討論利弊得失。
例如,A+B適用的對象是肝硬化分級Child-Pugh A者,那分級為B的人可以用嗎?因為缺乏臨床試驗,目前沒有定論。不只是免疫加標靶,蕾莎瓦、樂衛瑪這些標靶藥物當初的臨床實驗也沒有納入肝功能不好、肝功能為Child-Pugh B級的病人,因他們身體狀況較不穩定,接受抗癌治療容易產生副作用,不管是標靶藥物或是免疫藥物,都很難進行完整的隨機分配臨床試驗來驗證新治療的效果與安全性。目前僅有美國國家癌症資訊網(National Comprehensive Cancer Network, NCCN)根據上市後的追蹤研究報告或非隨機分配臨床試驗結果,建議針對Child B 級的肝癌病患,可以考慮使用A+B或是保疾伏(nivolumab)。然而因為個別病患狀況差異很大,必須非常謹慎與病患及家人討論可能的利弊得失。
有效者應用藥多久?沒有標準答案
使用A+B後,如何得知有效?由於接受A+B治療的病人是每三周注射一次藥物,至少做完三個療程才能觀察到效果,所以臨床上醫師也會安排病人在三個療程後做一次電腦斷層檢查,評估腫瘤是否有縮小。健保規定每次申請藥物以12周為限,之後會視療效如何,再決定要不要繼續向健保申請。
如果有效的話,要使用多久?健保條文為:「給付時程期限自初次處方用藥日起算2年。」實際上,這與當初A+B的臨床試驗設計不同,所以當健保給付期限一到,病人是否就應該停用?停用之後改採取什麼治療?這些都還沒有答案。
至於使用A+B無效的病人,健保已無藥物可銜接,自費使用蕾莎瓦、樂衛瑪或癌瑞格是可能的選項。
雙免疫療法即將引進國內
除了免疫加標靶外,美國食品藥物管理局(FDA)於2022年10月通過一個新的雙療法免疫組合(durvalumab+tremelimumab),亦可作為無法切除之肝細胞癌患者的第一線治療。其中,durvalumab(商品名:Imfinzi 抑癌寧)是抗PD- L1的免疫檢查點抑制劑,tremelimumab是抗CTLA-4免疫檢查點抑制劑(此藥國內尚未上市)。在一項名為HIMALAYA study的臨床試驗中,雙免疫治療的整體存活時間中位數(OS)為 16.4 個月,對照組使用蕾莎瓦治療為13.8 個月,具有統計學顯著的差距和具有臨床意義的改善。
此款雙免疫療法還在申請國內藥證及後續健保給付,如果順利通過,應與A+B同樣列在晚期肝癌的第一線療法,這兩種如何選擇?目前主要的考量是,當病人有出血風險,也就是胃鏡檢查有出血疑慮,不適合用A+B時,就可以選擇雙免疫療法。
全身性治療後有機會局部治療 肝癌的治療有分局部和全身性治療,原則上當肝癌還限縮在局部時,會以局部治療為主,包括開刀、電燒、栓塞、放射線等療法都屬於此類;若腫瘤已侵犯大血管(包括門靜脈或其他血管),標準治療就是藥物,也就是全身性療法,標靶藥物或免疫療
法都屬於全身性治療。
目前大家熱烈討論的臨床議題是,如果搭配局部治療與全身性藥物治療,是否能進一步改善晚期肝癌的治療效果?最好的情況是,病人使用A+B有效,腫瘤縮小到一定程度,身體條件各方面又許可下,可以接受開刀或其他的局部治療,將剩下的腫瘤消滅殆盡。能夠開刀是最好的,因為可以一勞永逸,無需用藥用到「天長地久」,臨床上也確實有這樣的病例。然而,這樣的病人畢竟還是少數,目前也還沒有可靠的生物指標(biomarkers)預測什麼樣的病人會如此好運。
放射治療也有角色 提升晚期肝癌治癒率
在醫學不斷進步下,放射治療能夠使用的武器也愈來愈多元,包括光子、質子、重粒子及釔90微球體放射線治療,讓晚期肝癌病人增添希望。
臨床上被轉介去做放射治療的晚期肝癌病人,大部分都已接受過藥物治療,放射科評估後可以利用放射治療破壞一些腫瘤,改善病人因為腫瘤長大、壓迫神經導致的疼痛症狀。
除此之外,放射治療還有一些情形可以派上用場,例如還沒有用過樂衛瑪或蕾莎瓦治療的病人,根據現行健保規定可以使用免疫加標靶,但如果病人有出血風險,那怎麼辦?或是有一些病人已經用過藥物治療一段時間,效果變差了,接下來呢?這些情況可以尋求放射治療的可能性,由放射治療科醫師跟病人解釋目前放射治療可能有什麼好處,有哪些選擇,與腫瘤科醫師合力,盡量控制住病情。新的質子或重粒子治療,可能對部分患者產生明顯療效。期待接下來能有更多臨床試驗,釐清這些新治療技術在肝癌照護的定位。
|


 字體:小 中 大
字體:小 中 大

 字體:小 中 大
字體:小 中 大